The importance of a DLMO-measurement when starting and stopping melatonin in minors
Background Melatonin is used as a chronobiotic in the treatment of sleeping disorders to correct disturbances in the circadian rhythm, including in children and adolescents. dim light melatonin onset (DLMO) and the peak in plasma concentration of melatonin contribute to this circadian rhythm. International research shows that the number of prescriptions for melatonin among children and adolescents is increasing significantly. However, there appears to be little empirical research on the best way to taper and/or discontinue melatonin in this population.
Aim To assess the available literature regarding the best way to taper and/or discontinue melatonin in minors with sleep problems, with or without autism spectrum disorder (ASD) or attention-deficit/hyperactivity disorder (ADHD).
Method A systematic review of the literature in the PubMed (Medline) and Embase databases.
Results Several effects of the melatonin therapy on sleep onset, sleep latency, sleep duration, sleep efficiency, and nocturnal activity disappear after discontinuation of the treatment. However, we cannot formulate evidence-based guidelines regarding treatment duration, timing of administration, dosage, or the method of discontinuation. DLMO prior to treatment does, however, have predictive value for the effect of discontinuing melatonin therapy.
Conclusion A DLMO-measurement prior to starting melatonin treatment provides clinicians with insight into the expected effects of melatonin during therapy. This allows for an estimation of whether melatonin will have not only a soporific but also a chronobiotic effect during treatment. Based on this information, clinicians can consider whether initiating or discontinuing melatonin therapy is appropriate. Consequently, our literature review provides a strong argument for reimbursement of DLMO-measurements by health insurance funds.
Melatonine is een endogeen hormoon dat geproduceerd en uitgescheiden wordt door de pijnappelklier. Het hormoon heeft een belangrijke functie in het circadiaan ritme en wordt voornamelijk tijdens de nacht vrijgemaakt, met een maximale plasmaconcentratie tussen 03:00 en 04:00 uur. De start van de melatonineproductie bij het aanbreken van de avond, onder schemerlicht, wordt dim light melatonin onset (DLMO) genoemd.1 DLMO en de piek in de plasmaconcentratie van melatonine vormen belangrijke endogene cues voor ons lichaam om over te gaan van waak tot slaap, hierdoor heeft het een chronobiotisch effect. Buiten het chronobiotisch effect heeft melatonine ook een slaapbevorderend effect, waarbij het de waakbevorderende signalen vanuit de nucleus suprachiasmaticus afzwakt.2 DLMO verschilt van individu tot individu, en kan ook variëren van dag tot dag door externe factoren (bijv. blootstelling aan licht). DLMO-bepalingen worden gebruikt om een verstoring in het circadiaan ritme te objectiveren.3
Het gebruik van melatonine kan onderdeel uitmaken van de behandeling voor slaapproblemen, ook bij kinderen en jongeren. De doeltreffendheid van melatonine bij kinderen en jongeren met slaapproblemen is voornamelijk onderzocht bij minderjarigen met een ontwikkelingsstoornis zoals autismespectrumstoornis (ASS) of aandachtsdeficiëntie-/hyperactiviteitsstoornis (ADHD), ontwikkelingsstoornissen waarbij een verhoogde prevalentie van slaapproblemen is aangetoond.4-7
Momenteel is het gebruik van melatonine als geneesmiddel bij minderjarigen in België en Nederland echter offlabel, tenzij in Nederland bij kinderen vanaf 2 jaar, met een diagnose ASS en/of smith-magenissyndroom, die last hebben van slapeloosheid.8 Er ontbreken tevens duidelijke, en wetenschappelijk onderbouwde, internationale richtlijnen die de clinicus kunnen gidsen in het verantwoord voorschrijven van melatonine bij minderjarigen.9
De auteurs van een overzichtsartikel uit 2014, gebaseerd op expertconsensus, formuleerden wel enkele richtlijnen rond zowel het starten als stopzetten van melatonine bij kinderen en jongeren.10 In dit artikel onderstrepen zij dat de evidentie voor het gebruik van dit middel voornamelijk berust op het gebruik bij kinderen en jongeren met een aangetoonde verstoring in het circadiaan ritme. Bijgevolg raden ze een DLMO-bepaling aan, om zo een verschuivingen van de DLMO te kunnen objectiveren, alvorens een behandeling met melatonine op te starten.
Deze auteurs beschrijven het gebruik van melatonine volgens twee verschillende invalshoeken. De eerste invalshoek is het gebruik van melatonine als chronobioticum om de verstoring in het circadiaan ritme te corrigeren door de plasmaconcentratie ervan toe te laten nemen op een tijdstip dat meer past bij een leeftijdsadequaat circadiaan ritme. Het artikel duidt 2 à 3 uur voor de DLMO aan als het optimaal tijdstip om melatonine toe te dienen of 3 à 4 uur voor het gewenst slaapuur indien er geen DLMO-bepaling uitgevoerd kan worden.
De tweede invalshoek berust niet op het effect van melatonine als chronobioticum, maar op het slaapverwekkend effect ervan. Wanneer melatonine als inslaper gebruikt wordt, ligt het ideale tijdstip van inname 30 minuten voor het gewenste slaapuur. De ideale dosering van melatonine wordt individueel bepaald. De auteurs beschrijven een dosering van 0,2-5 mg wanneer het als chronobioticum gebruikt wordt en van 1-3 mg wanneer het als inslaper gebruikt wordt. Daarbij adviseren zij een therapieduur van minstens een maand, zowel bij gebruik als chronobioticum als bij gebruik als inslaper, en verder individueel bepaald door periodes in te bouwen waarbij melatonine stopgezet wordt en vervolgens wordt geëvalueerd of de slaapproblemen terugkeren.10
Internationaal onderzoek toont aan dat het aantal voorschriften voor melatonine bij kinderen en jongeren sterk toeneemt.11,12 In België en Nederland zijn er dan ook veel kinderen en jongeren die langdurig gebruiker zijn van dit geneesmiddel.13 Er lijkt weinig empirisch onderzoek te bestaan over de effecten van de behandelduur en de beste manier om melatonine af te bouwen en/of stop te zetten. Aan de hand van een systematisch literatuuronderzoek trachten we de beschikbare evidentie daarover bij kinderen en jongeren met slaapproblemen, al dan niet met een diagnose ASS en/of ADHD, in kaart te brengen.
METHODE
We voerden een systematisch literatuuronderzoek uit in PubMed (Medline) en Embase, volgens de Preferred Reporting Items for Systematic reviews and Meta-Analyses(PRISMA)-richtlijnen, waarbij we gebruikmaakten van de zoekstring: (child*[Title/Abstract] OR paediatric[Title/Abstract] OR adolescen* [Title/Abstract] OR baby[Title/Abstract] OR babies[Title/Abstract] OR infan*[Title/Abstract]) AND (sleep*[MeSH Terms] OR sleep*[Title/Abstract] OR insomnia[MeSH Terms] OR insomnia[Title/Abstract]) AND (melatonin[Title/Abstract] OR melatonin[MeSH Terms]) voor de zoekopdracht op PubMed en de zoekstring: (‘child*’:ti,ab,kw OR ‘paediatric’:ti,ab,kw OR ‘adolescen*’:ti,ab,kw OR ‘baby’:ti,ab,kw OR ‘babies’:ti,ab,kw OR ‘infan*’:ti,ab,kw) AND (‘sleep*’ OR ‘sleep*’:ti,ab,kw OR ‘insomnia’/exp OR ‘insomnia’:ti,ab,kw) AND (‘melatonin’:ti,ab,kw OR ‘melatonin’/exp) voor de zoekopdracht op Embase.
Bij beide zoekopdrachten includeerden we alleen artikelen waarin duidelijk beschreven werd wanneer melatonine stopgezet of afgebouwd werd na een behandeling van slaapproblemen bij kinderen of adolescenten en wat het effect van het stopzetten of afbouwen van het geneesmiddel op de slaapparameters was.
We excludeerden studies waarbij de studiepopulatie uitsluitend bestond uit kinderen en jongeren met een syndromale ontwikkelingsstoornis of andere aandoeningen die invloed kunnen hebben op het slaappatroon. Wel includeerden we studies waarbij de gehele studiepopulatie of een deel ervan, naast enkel slaapproblemen, ook een diagnose ASS en/of ADHD had. Ook namen we enkel artikelen op die origineel onderzoek betroffen en geschreven waren in het Engels of Nederlands.
De laatste zoekopdracht op beide databanken werd uitgevoerd op 20 november 2024. De eerste auteur (MB) voerde de zoekopdracht uit, screende titels en abstracts en nam de tekst van de artikelen door.
RESULTATEN
De zoekopdracht leverde in totaal 3056 resultaten op (873 in PubMed en 2183 in Embase). Na screening van titel en abstract bleven er 45 artikelen over die in zijn geheel doorgenomen werden. Van de doorgenomen artikelen voldeden er 9 aan de in- en exclusieclusiecriteria (zie figuur 1 en onlinetabel 1).14-22
Figuur 1. PRISMA-stroomdiagram literatuurzoekopdracht
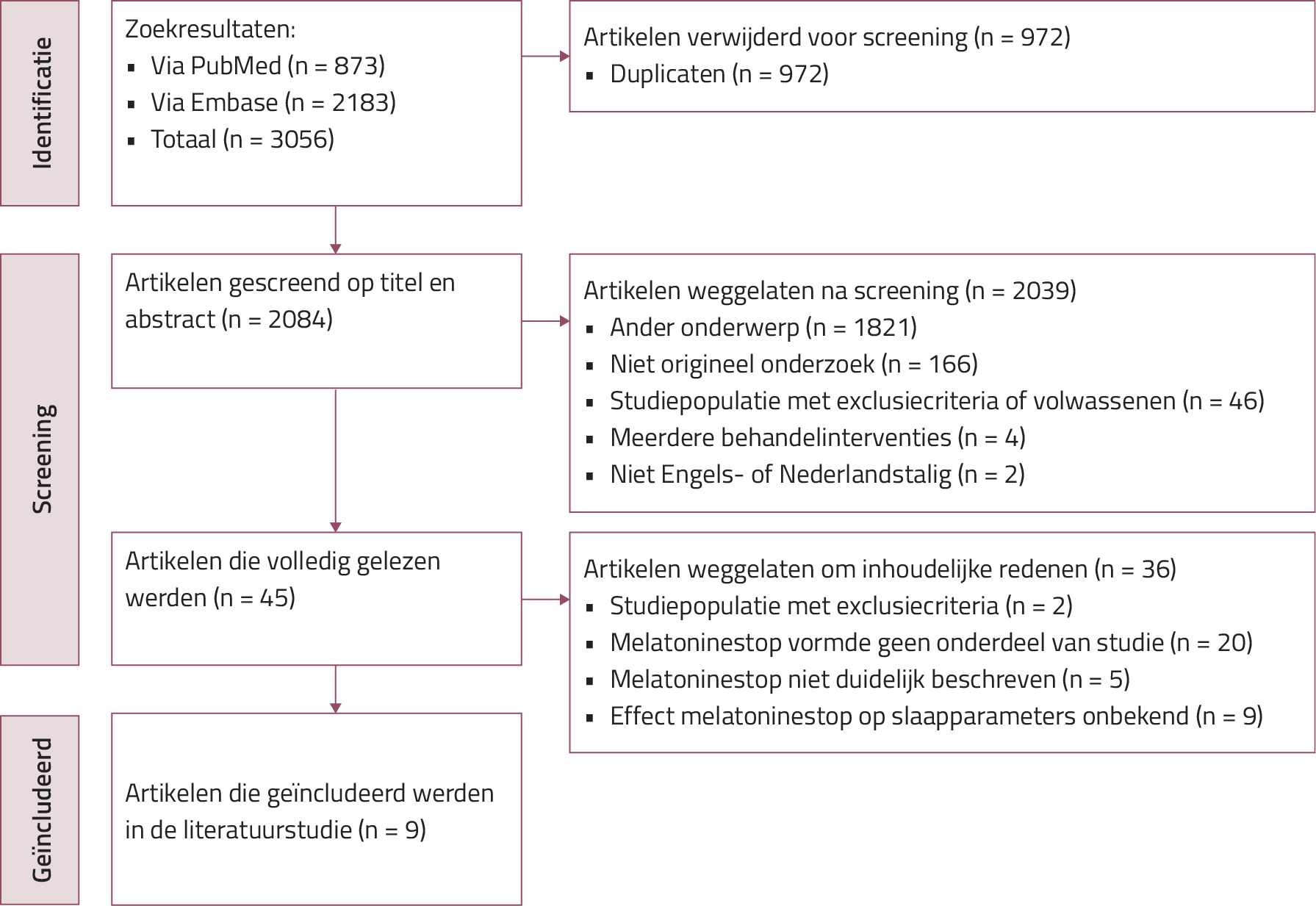
De geïncludeerde studies werden gepubliceerd tussen 2003 en 2022 en betroffen in totaal 563 patiënten, waarbij melatonine bij 462 patiënten werd stopgezet (voor demografische gegevens zie onlinetabel 1).
Tabel 1. Geïncludeerde studies
|
Eerste auteur (jaar) |
Type onderzoek |
Studie-populatie, aantal waarbij melatonine (tijdelijk) stopgezet werd |
Comorbiditeit |
Gem. leeftijd (uitersten), in j |
Verhouding jongens/meisjes |
Duur melatoninebehandeling |
Tijdstip van toediening |
Dosering (vorm) |
Tijd tussen stop en evaluatie |
Meet-instrumenten |
Gerapporteerd effect van (tijdelijke) stop/afbouw melatonine |
|---|---|---|---|---|---|---|---|---|---|---|---|
|
Giannotti (2006) |
Open label prospectief |
Studie: n = 29 Stopzetting: n = 23 |
ASS |
4,3 |
25/4 |
6 m |
20:00 u |
1 mg (FR) + 2 mg (CR) -6 mg (FR+CR) |
3 w of 1 m |
CSHQ; slaapdagboek |
Verandering in CSHQ: terugkeer naar waarden voor behandeling: n = 16 (67 vs. 73; NS); aanhoudende verbetering CSHQ-waarden: n = 4 (57 vs. 47: p < 0,001) |
|
Hayashi (2022) |
Open label prospectief na RCT |
Studie: n = 196 Stopzetting: n = 188 |
ASS |
11,2 (-) |
121/75 |
6 of 8 w |
45 min voor gewenst slaapuur |
1, 2 of 4 mg (NAO) |
2 w |
Actometer; slaapdagboek |
Mediaan slaaplatentie (slaapdagboek): toename na stopzetting (-27 vs. -10 min) |
|
van Maanen (2011) |
Open label prospectief |
Studie: n = 41 Stopzetting: n = 41 |
ADHD: n = 8; ASS: n = 5 ADHD en ASS: n = 1 |
9,43 |
24/17 |
3 w |
19:00 u |
1-5 mg (FR) |
1 w |
Actometer; slaapdagboek; DLMO-meting |
Gem. slaaplatentie: toename na stopzetting (37,27 vs. 69,39 min; p < 0,001) Gem. slaapstart: later na afbouw (21:00 vs. 21:11 u; p = 0,002); later na stopzetting (21:00 vs. 21:43 u; p < 0,001) Gem. slaapduur: afname na afbouw (8,60 vs. 8,48 u; p = 0,044); afname na stopzetting (8,60 vs. 8,13 u; p < 0,001) Gem. slaapefficiëntie: afname na stopzetting (75,72 vs. 72,34%; p < 0,001) Gem. DLMO: later na stopzetting (19:31 vs. 20:55 u; p < 0,001) |
|
van Maanen (2017) |
Open label prospectief |
Studie: n = 16 Stopzetting: n = 16 |
ADHD: n = 4; ADHD en ASS: n = 1 |
9,92 (-) |
6/10 |
3 w |
19:00 u |
1-5 mg (FR) |
1 w |
Actometer; slaapdagboek; DLMO-meting |
Gem. slaaplatentie: toename na stopzetting (41,97 vs. 66,13 min) Gem. slaapstart: later na stopzetting (21:35 vs. 22:18 u) Gem. slaapduur: afname na stopzetting (8,42 vs. 8,00 u) Gem. slaapefficiëntie: afname na stopzetting (78,28 vs. 74,76%) Gem. DLMO: later na stopzetting (20:03 vs. 20:43 u) |
|
Malow (2021) |
Open label prospectief na RCT |
Studie: n = 119 Stopzetting: n = 73 |
ASS: n = 70; SMS: n = 3 |
- (2-17,5) |
- |
91 w of 104 w |
30-60 min voor gewenst slaapuur |
2, 5 of 10 mg (PedPRM) |
2 w |
Slaapdagboek; CSDI; PSQI |
Verandering in CSDI: gedeeltelijke terugkeer naar waarden voor behandeling |
|
Paavonen (2003) |
Open label prospectief |
Studie: n = 15 Stopzetting: n = 14 |
ASS: n = 15 |
- (6-17) |
13/2 |
2 w |
30 min voor gewenst slaapuur |
3 mg (NOA) |
3,5 w |
Actometer; slaapdagboek; SDSC; KSS |
Gem. nachtelijke activiteit (actometer): toename na stopzetting (22,26 vs. 18,74; p = 0,023) Gem. slaapduur (actometer): afname na stopzetting (466,45 vs. 480,48 min; p = 0,034) |
|
Wright (2011) |
Open label, cross-over, prospectief |
Studie: n = 20 Stopzetting: n = 16 |
ASS: n = 20 |
9 (4-16) |
16/4 |
3 m |
30-40 min voor gewenst slaapuur |
2 en 10 mg (FR) |
1 m |
Slaapdagboek |
Gem. slaaplatentie (slaapdagboek): toename na stopzetting |
|
Hoebert (2009) |
Retrospectieve follow-up na RCT |
Studie: n = 94 Stopzetting: n = 67 (22 definitieve stopzetting; 45 tijdelijke stopzetting) |
ADHD |
12,39 (-) |
70/24 |
1-57 m |
18:30-23:00 u |
0,5 en 10 mg (FR) |
Variabel |
Vragenlijst (NAO); DLMO-meting (uitgevoerd tijdens RCT) |
DLMO-verandering: DLMO voor behandeling vroeger bij groep zonder terugval CSOI na definitieve stopzetting behandeling dan bij groep die nog behandeld werd met melatonine (20:21 vs. 20:41 u; p = 0,413) Terugval in CSOI bij stopzetten: n = 14 wel vs. n = 8 geen terugval |
|
Zwart (2018) |
Retrospectieve follow-up na RCT |
Studie: n = 33 Stopzetting: n = 24 |
- |
19,6 (16,7-23,2) |
14/19 |
1-11,9 j |
19:00-23:00 u (bij patiënten die wel nog behandeld werden met melatonine) |
Dosering en vorm niet beschreven |
Variabel |
Vragenlijst (NAO); MEQ; MCTQ; PSQI; ISI |
Slaappatroon op volwassen leeftijd: vergelijkbaar met populatie die geen last had van slaapproblemen voor volwassen leeftijd |
ASS: autismespectrumstoornis; FR: fast release; CR: controlled release; CSHQ: Children’s Sleep Habits Questionnaire; RCT: gerandomiseerde gecontroleerde trial; NAO: niet anders omschreven; ADHD: aandachtsdeficiëntie-/hyperactiviteitsstoornis; DLMO: dim light melatonin onset; SMS: smith-magenissyndroom; PedPRM: pediatric prolonged-releasemelatonine; CSDI: Composite Sleep Disturbance Index; PSQI: Pittsburgh Sleep Quality Index; SDSC: Sleep Disturbance Scale for Children; KSS: Karolinska Sleepiness Scale; CSOI: Chronic Sleep Onset Insomnia; MEQ: Morningness-Eveningness Questionnaire; MCTQ: Munich Chronotype Questionnaire; ISI: Insomnia Severity Index.
Onderzoeksopzet en -procedure
Van de 9 artikelen betroffen er 7 de resultaten van een klinische studie en 2 de resultaten van een retrospectief onderzoek (zie onlinetabel 1). Binnen de 7 klinische studies verschilde de therapieduur sterk: van minimaal 2 tot maximaal 104 weken (2 jaar). In beide retrospectieve onderzoeken kon men geen specifieke therapieduur definiëren daar de stop van melatonine geen gepland onderdeel uitmaakte van de studieprocedure.21,22 Het tijdstip van inname varieerde binnen de 7 klinische studies; in studies met een vast toedieningsmoment varieerde de inname tussen 19:00 en 20:00 uur, bij studies met individueel afgestemde inname vond inname plaats 30-60 minuten voor het gewenste slaapuur. Binnen de 2 retrospectieve onderzoeken varieerde het tijdstip van inname bij patiënten die nog behandeld werden met melatonine tussen 18:30 en 23:00 uur.21,22 De dosering varieerde, zowel tussen de verschillende studies als binnen de verschillende studiepopulaties, tussen 0,5 mg en 10 mg.
Verschillende vormen van melatonine werden toegediend: een snelwerkende vorm (melatonine FR), een vorm met gecontroleerde afgifte (melatonine CR) en een vorm met een verlengde afgifte die speciaal ontworpen is voor kinderen (PedPRM). In beide studies, uitgevoerd door Van Maanen e.a., halveerden de onderzoekers eerst de dosering van melatonine gedurende een week vooraleer het volledig stopgezet werd.16,17 De overige studies beschreven dat melatonine meteen volledig stopgezet werd.
Effecten van de afbouw en stopzetting van melatonine
In 3 studies rapporteerde men uitkomsten van DLMO-metingen. In hun twee studies toonden Van Maanen e.a. aan dat DLMO vroeger plaatsvond tijdens de behandeling, maar dat DLMO weer later op de avond plaatsvond 1 week na het stopzetten van de behandeling.16,17 Hoebert e.a. konden aantonen dat DLMO voor de behandeling doorgaans vroeger was bij een fractie van patiënten (36%) die de behandeling succesvol konden stopzetten.21 In 3 van de 4 studies waarin men actometers gebruikte, werd aangetoond dat na het stopzetten van de behandeling de effecten op slaapstart, -latentie, -duur en -efficiëntie en nachtelijke activiteit wegvielen (zie onlinetabel 1). 16,17,19
In 8 van de 9 studies konden de onderzoekers aan de hand van subjectieve uitkomstmaten duidelijk aantonen dat het afbouwen en/of stopzetten van de behandeling met melatonine een negatieve invloed had op slaapstart, -latentie, -duur en -efficiëntie (zie onlinetabel 1). Enkel Zwart e.a. rapporteerden dat circa 75% van de patiënten binnen de studiepopulatie bij wie melatonine opgestart werd na 10 jaar een normale slaapkwaliteit had zonder dit middel.22
Van Maanen e.a. halveerden in hun studies de dosering eerst gedurende een week vooraleer melatonine volledig stopgezet werd. Hoewel slaapefficiëntie en -latentie minder negatief beïnvloed werden na een halvering van de dosering, werd er na het stopzetten van de behandeling geen verschillend effect op slaaplatentie en -efficiëntie geobserveerd in vergelijking met het plots stopzetten van de behandeling.16,17
BESPREKING
Aan de hand van dit systematisch literatuuroverzicht wordt aangetoond dat de effecten van een behandeling met melatonine op slaapstart, -latentie, -duur en -efficiëntie en nachtelijke activiteit wegvallen nadat deze behandeling stopgezet wordt. Ook de verandering in DLMO, die na een behandeling met melatonine vroeger op de avond plaatsvindt, valt geleidelijk aan weg nadat melatonine stopgezet wordt. Therapieduur, tijdstip van inname, dosering en de manier van stopzetten lijken geen invloed te hebben op het effect van het stopzetten van de behandeling met melatonine.14-20
Hierbij dienen we wel te vermelden dat we, na het samenbrengen van de resultaten van de verschillende geïncludeerde studies, geen bijkomende analyses verricht hebben om deze uitspraak statistisch te kunnen onderbouwen. We kunnen aan de hand van dit systematisch literatuuroverzicht dan ook geen wetenschappelijk onderbouwde richtlijnen formuleren over therapieduur, tijdstip van inname, dosering en de manier van stopzetten.
Er wordt echter een fractie van patiënten beschreven (36,3%) die de behandeling met melatonine succesvol kon stopzetten zonder terugkeer van de slaapproblemen. Binnen de fractie die de behandeling succesvol kon stopzetten, kon aangetoond worden dat DLMO voor de behandeling doorgaans vroeger was, en dat er bijgevolg een minder ernstige verstoring van het circadiaan ritme was voor de behandeling, dan bij de patiënten die nog behandeld werden met melatonine. Deze uitspraak berust echter op slechts 1 retrospectief onderzoek met een kleine groep patiënten waarbij melatonine stopgezet werd (n = 67).20 Het middel kon wel stopgezet worden, zonder terugkeer van de slaapproblemen, indien het circadiaan ritme weer samenvalt met het gewenste dag-nachtritme. Hierbij wordt het wegvallen van de slaapproblemen niet toegeschreven aan het effect van de behandeling maar wel aan de verandering van het slaappatroon bij het volwassen worden. Ook deze uitspraak berust op 1 retrospectief onderzoek met een kleine patiëntenpopulatie (n = 33).22
Adviezen
Aan de hand van de resultaten van dit systematisch literatuuroverzicht adviseren we om voor het starten van een behandeling met melatonine bij kinderen en jongeren met slaapproblemen een DLMO-bepaling uit te voeren. Wanneer er geen verstoring van de DLMO, en bijgevolg van het circadiaan ritme, geobjectiveerd kan worden voor de start van de behandeling, kan men aannemen dat de werking van melatonine tijdens de behandeling voornamelijk slaapverwekkend is en kan men veronderstellen dat de oorzaak van de slaapproblemen eerder toe te schrijven is aan externe factoren (bijv. aanpassingen aan het gewenste slaapuur of gebeurtenissen die stress veroorzaken en invloed hebben op het slaappatroon).
Wanneer deze externe factoren wegvallen, is de kans groter dat een behandeling met melatonine stopgezet kan worden, zonder een terugkeer van de slaapproblemen. Indien er wel een (ernstige) verstoring van de DLMO, en bijgevolg van het circadiaan ritme, geobjectiveerd kan worden voor de start van de behandeling, kan men stellen dat de effecten van een behandeling met melatonine niet enkel berusten op het slaapverwekkend effect van het geneesmiddel. Zo zal in dit geval melatonine, naast een slaapverwekkend, ook een chronobiotisch effect hebben. Bij het stopzetten van de behandeling valt dan zowel het slaapverwekkend als het chronobiotisch effect van melatonine weg, waardoor de kans groter is dat er een terugkeer is van de slaapproblemen.
Vergoeding van DLMO-bepaling
Een DLMO-bepaling is kostbaar en wordt binnen België en Nederland niet terugbetaald door de mutualiteit resp. zorgverzekeraar. Ook staat de rol van een afwijkende DLMO binnen primaire slaap-waakstoornissen ter discussie. Zo wordt in de DSM-5 vermeld dat een DLMO-meting niet wenselijk is.23
Binnen de International Classification of Sleep Disorders (ICSD) wordt er echter, naast een onderscheid tussen slaapstoornissen die wel of niet toe te schrijven zijn aan een verstoring van het circadiaan ritme aan de hand van een DLMO-meting, ook verder onderscheid gemaakt naargelang het type verschuiving van de DLMO.24 Bijkomend kan men het tijdstip van inname bij een behandeling met melatonine het beste bepalen aan de hand van de individuele DLMO, omdat dit ook invloed heeft op de doeltreffendheid van de behandeling.24 Verschillende onderzoekers pleiten hierdoor reeds voor het standaard uitvoeren van een DLMO-bepaling voor de start van een behandeling met melatonine.10,24
Ons literatuuronderzoek biedt hiernaast ook een sterk argument voor de vergoeding van DLMO-bepalingen door de mutualiteit resp. zorgverzekeraar. Men kan namelijk aan de hand van een DLMO-bepaling, voor de start van een behandeling met melatonine, onderzoeken of het naast een slaapverwekkend ook een chronobiotisch effect zal hebben tijdens de behandeling. Aan de hand van deze informatie kan men vervolgens de kans inschatten dat de slaapproblemen terugkeren na het stopzetten van de behandeling, en kan men overwegen of het stopzetten van de behandeling wenselijk is.
Aanbevelingen voor verder onderzoek
De resultaten en conclusie die voortkomen uit onze onderzoeksvraag geven in eerste instantie verdere inzichten en overwegingen rond het stopzetten van een melatoninebehandeling. Hiernaast komen we tevens tot een aantal vragen die verder onderzoek kunnen gidsen en die relevant zijn in de overweging om een behandeling met melatonine, als chronobioticum, voor slaapproblemen bij kinderen en jongeren te starten.
Een van de vragen die de resultaten van dit systematisch literatuuronderzoek oproept, is of men kan verwachten dat een behandeling met melatonine zorgt voor blijvende (neurobiologische) veranderingen die leiden tot een blijvende verbetering van het slaappatroon, ook na het stopzetten van de behandeling. Momenteel is er enkel grondig wetenschappelijk onderzoek voorhanden naar de invloed van een behandeling met melatonine op DLMO.25 Er ontbreekt grondig wetenschappelijk onderzoek dat andere (neurobiologische) veranderingen, na een behandeling met melatonine, in kaart brengt.
Ook moeten normale variaties in DLMO binnen de populatie, eventuele genetische invloeden, maar ook veranderingen in DLMO van de kindertijd naar volwassenheid, in overweging genomen worden. Eerder onderzoek kon aantonen dat DLMO, in vergelijking met die binnen de volwassen populatie, doorgaans vroeger op de avond plaatsvindt bij kinderen van 0-9 jaar, en later op de avond bij jongeren en adolescenten van 10-19 jaar.2 De vraag is dan ook of we dit gelijk kunnen stellen met een pathologische afwijking van het circadiaan ritme. Een andere belangrijke overweging is of een behandeling met melatonine als chronobioticum de meest aangewezen keuze is voor het behandelen van slaapproblemen bij kinderen en jongeren, met een afwijking in het circadiaan ritme en DLMO die tijdens het opgroeien zal normaliseren of samen zal vallen met het gewenste dag-nachtritme.22
Sterke punten en beperkingen
Ons systematische literatuuronderzoek is, voor zover ons bekend, het eerste waarin evidentie in kaart wordt gebracht om het stopzetten van melatonine bij kinderen en jongeren met slaapproblemen, wetenschappelijk te onderbouwen en van hieruit implicaties voor de klinische praktijk te formuleren.
We dienen wel op te merken dat ons literatuuronderzoek enkele beperkingen heeft. Zo vonden we slechts 9 studies die voldeden aan de vooropgestelde in- en exclusiecriteria. Hierdoor betreft ons literatuuronderzoek een relatief beperkte patiëntenpopulatie. Studieprocedures varieerden ook sterk binnen de geïncludeerde artikelen waarbij er ook sprake was van een sterke variatie in therapieduur, dosering en tijdstip van inname. Het ontbreken van gerandomiseerde gecontroleerde trials maakt ook dat we geen uitspraken kunnen doen over eventuele placebo-effecten, waardoor we deze niet mee in overweging hebben kunnen nemen.
CONCLUSIE
Ons systematisch literatuuroverzicht toont aan dat de effecten van een behandeling met melatonine op slaapstart, -latentie, -duur en -efficiëntie en nachtelijke activiteit wegvallen nadat deze behandeling wordt stopgezet. We kunnen echter geen wetenschappelijk onderbouwde richtlijnen formuleren betreffende therapieduur, tijdstip van inname, dosering en de manier van stopzetten.
Een DLMO-bepaling voor het starten van een behandeling met melatonine geeft de clinicus zicht op het effect ervan tijdens de behandeling. Zo kan men inschatten of melatonine naast een slaapverwekkend ook een chronobiotisch effect zal hebben tijdens de behandeling. Aan de hand van deze informatie kan men overwegen of het starten of stopzetten van deze behandeling wenselijk is. Hierdoor biedt ons literatuuronderzoek een sterk argument voor de vergoeding van DLMO-bepalingen door de mutualiteit resp. de zorgverzekeraar.
Literatuur
1 Claustrat B, Brun J, Chazot G. The basic physiology and pathophysiology of melatonin. Sleep Med Rev 2005; 9: 11-24.
2 Van Gastel A, Neu D. Slaapstoornissen. In: Dierick M, Claes S, De Nayer, e.a., red. Handboek psychofarmacotherapie. Gent: Academia Press; 2012. p. 235-61.
3 Kennaway DJ. The dim light melatonin onset across ages, methodologies, and sex and its relationship with morningness/eveningness. Sleep 2023; 46: 1-14.
4 Richdale AL, Schreck KA. Sleep problems in autism spectrum disorders: Prevalence, nature, & possible biopsychosocial aetiologies. Sleep Med Rev 2009; 13: 403-11.
5 Owens JA. The ADHD and sleep conundrum: a review. J Dev Behav Pediatr 2005; 26: 312-22.
6 Abdelgadir IS, Gordon MA, Akobeng AK. Melatonin for the management of sleep problems in children with neurodevelopmental disorders: a systematic review and meta-analysis. Arch Dis Child 2018; 103: 1155-62.
7 Wei S, Smits MG, Tang X, e.a. Efficacy and safety of melatonin for sleep onset insomnia in children and adolescents: a meta-analysis of randomized controlled trials. Sleep Med 2020; 68: 1-8.
8 Christiaens T, Maloteaux JM. Melatonine bij kinderen met slapeloosheid. BCFI; Folia Pharmacotherapeutica 2021; 48: 1-6.
9 Edemann-Callesen H, Andersen HK, Ussing A, e.a. Use of melatonin for children and adolescents with chronic insomnia attributable to disorders beyond indication: A systematic review, meta-analysis and clinical recommendation. eClinicalMedicine 2023; 61: 102049.
10 Bruni O, Alonso-Alconada D, Besag F, e.a. Current role of melatonin in pediatric neurology: Clinical recommendations. Eur J Paediatr Neurol 2014: 1-12.
11 Hartz I, Handal M, Tverdal A, e.a. Paediatric off-label use of melatonin – a register linkage study between the Norwegian Prescription Database and Patient Register. Basic Clin Pharmacol Toxicol 2015; 117: 267-73.
12 Kimland EE, Bardage C, Collin J, e.a. Pediatric use of prescribed melatonin in Sweden 2006-2017: a register based study. Eur. Child Adolesc Psychiatry. 2021; 30: 1339-50.
13 Koopman-Verhoeff ME, van den Dries MA, van Seters JJ, e.a. Association of sleep problems and melatonin use in school-aged children. JAMA Pediatr 2019; 173: 883-85.
14 Giannotti F, Cortesi F, Cerquiglini A, e.a. An open-label study of controlled-release melatonin in treatment of sleep disorders in children with autism. J Autism Dev Disord 2006; 36: 741-52.
15 Hayashi M, Mishima K, Fukumizu M, e.a. Melatonin treatment and adequate sleep hygiene interventions in children with autism spectrum disorder: a randomized controlled trial. J Autism Dev Disord 2022; 52: 2784-93.
16 Van Maanen A, Meijer AM, Smits MG, e.a. Termination of short term melatonin treatment in children with delayed Dim Light Melatonin Onset: Effects on sleep, health, behavior problems and parenting stress. Sleep Med 2011; 12: 875-9.
17 Van Maanen A, Meijer AM, Smits MG, e.a. Classical conditioning for preserving the effects of short melatonin treatment in children with delayed sleep: a pilot study. Nat Sci Sleep 2017; 9: 67-79.
18 Malow BA, Findling RL, Schroder CM, e.a. Sleep, growth, and puberty after 2 years of prolonged-release melatonin in children with autism spectrum disorder. J Am Acad Child Adolesc Psychiatry 2021; 60: 252-61.
19 Paavonen EJ, Nieminen-von Wendt T, Vanhala R, e.a. Effectiveness of melatonin in the treatment of sleep disturbances in children with Asperger disorder. J Child Adolesc Psychopharmacol 2003; 13: 83-95.
20 Wright B, Sims D, Smart S, e.a. Melatonin versus placebo in children with autism spectrum conditions and severe sleep problems not amenable to behaviour management strategies: a randomised controlled crossover trial. J Autism Dev Disord 2011; 41: 175-84.
21 Hoebert M, van der Heijden KB, van Geijlswijk IM, e.a. Long-term follow-up of melatonin treatment in children with ADHD and chronic sleep onset insomnia. J Pineal Res 2009; 47: 1-7.
22 Zwart TC, Smits MG, Egberts TCG, e.a. Long-term melatonin therapy for adolescents and young adults with chronic sleep onset insomnia and late melatonin onset: evaluation of sleep quality, chronotype, and lifestyle factors compared to age-related randomly selected population cohorts. Healthcare 2018; 6: 23.
23 American Psychiatric Association. Handboek voor de classificatie van psychische stoornissen (DSM-5). Nederlandse vertaling van diagnostic and statistical manual of mental disorders, 5de ed. Amsterdam: Boom: 2014. p. 502-76.
24 Keijzer H, Smits MG, Duffy JF, e.a. Why the dim light melatonin onset (DLMO) should be measured before treatment of patients with circadian rhythm sleep disorders. Sleep Med Rev 2014; 18: 333-9.
25 Van Geijlswijk IM, Korzilius HPLM, Smits MG. The use of exogenous melatonin in delayed sleep phase disorder: a meta-analysis. Sleep 2010; 33: 1605-14.
Authors
Maarten Baens, tijdens het schrijven: arts in opleiding tot kinder- en jeugdpsychiater, UPC KU Leuven; thans: kinder- en Jeugdpsychiater, Zorggroep Myna.
Marina Danckaerts, hoogleraar Kinder- en jeugdpsychiatrie, dept. Neurowetenschappen, UPC KU Leuven.
Correspondentie
Maarten Baens (maarten.baens@zorggroepmyna.be).
Geen strijdige belangen gemeld.
Het artikel werd voor publicatie geaccepteerd op 13-10-2025.
Citeren
Tijdschr Psychiatr. 2026;68(2):70-74
